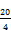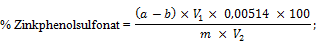Anlage 7
VII. NACHWEIS UND QUANTITATIVE BESTIMMUNG DER PHENOLSULFONSÄURE
- 1. ZWECK UND ANWENDUNGSBEREICH
Die Methode beschreibt die qualitative und quantitative Bestimmung der Phenolsulfonsäure in kosmetischen Erzeugnissen, z. B. in Aerosolen und Gesichtswässern.
- 2. DEFINITION
Die nach dieser Vorschrift bestimmte Phenolsulfonsäure wird in Massenprozent als Zinkphenolsulfonsäure (wasserfreie Substanz) ausgedrückt, siehe Punkt 11.
- 3. PRINZIP
Der zu analysierende Teil der Probe wird unter vermindertem Druck eingeengt, in Wasser gelöst und mit Chloroform extrahiert. Die Bestimmung der Phenolsulfonsäure erfolgt bromo-jodometrisch in einem aliquoten Teil der gereinigten und filtrierten wässerigen Lösung.
- 4. REAGENZIEN Alle Reagenzien müssen analysenrein sein.
- 4.1. Salzsäure, konz. 36 %ig
- 4.2. Chloroform
- 4.3. n-Butanol
- 4.4. Eisessig
- 4.5. Kaliumjodid
- 4.6. Kaliumbromid
- 4.7. Natriumcarbonat
- 4.8. Sulfanilsäure
- 4.9. Natriumnitrit
- 4.10. Kaliumbromatlösung: 0,1 N
- 4.11. Natriumthiosulfatlösung: 0,1 N
- 4.12. Stärkelösung: 1 %ig (m/v) in Wasser
- 4.13. Natriumcarbonatlösung: 2 %ig (m/v) in Wasser
- 4.14. Natriumnitritlösung: 4,5 %ig (m/v) in Wasser
- 4.15. Dithizonlösung: 0,05 %ig (m/v) in Chloroform
- 4.16. Fließmittel: n-Butanol-Eisessig-Wasser (4:1:5), v); nach dem Mischen im Scheidetrichter wird die untere Phase verworfen.
- 4.17. Reagenz nach Pauly für die Dünnschichtchromatographie: 4,5 g Sulfanilsäure (4.8) werden in 45 ml konzentrierter Salzsäure (4.1) unter Erwärmen gelöst und die Lösung mit Wasser auf 500 ml verdünnt. 10 ml der Lösung werden in Eiswasser gekühlt und unter Rühren 10 ml klare Natriumnitritlösung (4.14) zugesetzt. Danach läßt man die Lösung ca. 15 Minuten bei 0 °C stehen – die Lösung ist bei dieser Temperatur 1 bis 3 Tage stabil; kurz vor dem Besprühen (7.5) werden 20 ml Natriumcarbonatlösung (4.13) hinzugegeben.
- 4.18. Zellulosebeschichtete Fertigplatten für die Dünnschichtchromatographie; Format 20 x 20 cm, Dicke der Sorbtionsschicht 0,25 mm.
- 5. GERÄTE
- 5.1. Rundkolben mit Schliff: 100 ml
- 5.2. Scheidetrichter: 100 ml
- 5.3. Erlenmeyerkolben mit Schliff: 250 ml
- 5.4. Bürette: 25 ml
- 5.5. Vollpipetten: 1, 2 und 10 ml
- 5.6. Meßpipette: 5 ml
- 5.7. Injektionsspritze: 10
l mit 0,1 Mikroliterskala
- 5.8. Thermometer: Skala von 0 bis 100 °C
- 5.9. Wasserbad mit Heizung
- 5.10. Trockenofen: gut ventiliert und auf 80 °C eingestellt
- 5.11. Übliche Ausrüstung für die Dünnschichtchromatographie
- 6. PROBENVORBEREITUNG
Für die im folgenden beschriebene qualitative und quantitative Bestimmung der Phenolsulfonsäure in Aerosolen kann der Rückstand des Sprühdoseninhalts verwendet werden, der durch Abdestillation der flüchtigen Lösungs- und Treibmittel unter normalem Druck erhalten wird.
- 7. IDENTIFIZIERUNG
- 7.1. Auf der Startlinie – 1 cm über der unteren Kante der Dünnschichtplatte (4.18) – werden auf sechs Punkte mit einer Injektionsspritze (5.7) jeweils 5
l des Rückstandes (6) oder der Probe aufgetragen.
- 7.2. Die Platte wird in eine Entwicklungskammer mit dem Fließmittel (4.16) eingesetzt und so lange entwickelt, bis die Fließmittelfront 15 cm über der Startlinie erreicht hat.
- 7.3. Dann wird die Platte aus der Entwicklungskammer genommen, bei 80 °C getrocknet, bis keine Essigsäuredämpfe mehr wahrnehmbar sind, anschließend mit Natriumcarbonatlösung (4.13) besprüht und an der Luft getrocknet.
- 7.4. Die eine Hälfte der Platte wird mit einer Glasplatte abgedeckt und der nicht abgedeckte Teil mit 0,05%iger Dithizonlösung (4.15) besprüht. Zink-Ionen werden durch Bildung rotvioletter Flecke angezeigt.
- 7.5. Dann wird die bereits besprühte Hälfte mit Pauly-Reagens (4.17) besprüht. Die p-Phenolsulfonsäure (Rf-Wert etwa 0,26) wird als gelb-brauner, die m-Phenolsulfonsäure (Rf-Wert etwa 0,45) als gelber Fleck im Chromatogramm sichtbar.
- 8. QUANTITATIVE BESTIMMUNG
- 8.1. 10 g der Probe oder des Rückstandes (6) werden in einen 100-ml-Rundkolben eingewogen und mittels eines Rotationsverdampfers im Vakuum im Wasserbad von 40 °C annähernd zur Trocknung eingeengt.
- 8.2. Danach werden 10,0 ml (V1) Wasser in den Kolben einpipettiert und der Abdampfrückstand (8.1) in der Wärme gelöst.
- 8.3. Die Lösung wird in einen Scheidetrichter (5.2) quantitativ überführt und die wässerige Lösung zweimal mit jeweils 20 ml Chloroform (4.2) extrahiert; die Chloroformphase wird nach jeder Extraktion verworfen.
- 8.4. Die wässerige Lösung wird durch einen Papierfilter filtriert und je nach dem erwarteten Gehalt an Phenolsulfonsäure 1,0 oder 2,0 ml (V2) des Filtrats in einen 250-ml-Erlenmeyerkolben (5.3) eingegeben und mit destilliertem Wasser auf 75 ml verdünnt.
- 8.5. Anschließend werden 2,5 ml 36%ige Salzsäure (4.1) sowie 2,5 g Kaliumbromid (4.6) zugefügt, durchgemischt und die Lösung im Wasserbad auf 50 °C erwärmt.
- 8.6. Aus einer Bürette wird so viel 0,1 N Kaliumbromatlösung (4.10) hinzugefügt, bis die Farbe der 50 °C warmen Lösung nach gelb umschlägt.
- 8.7. Nach dem Zusatz weiterer 3,0 ml Kaliumbromatlösung (4.10) wird der Kolben verschlossen und 10 Minuten in ein Wasserbad (50 °C) eingestellt. Sollte nach 10 Minuten die Gelbfärbung der Lösung verschwunden sein, werden weitere 2,0 ml Kaliumbromatlösung (4.10) in den Kolben gegeben, dieser erneut mit dem passenden Stopfen verschlossen und weitere 10 Minuten in das Wasserbad eingestellt. Die Gesamtmenge (a) der zugegebenen Kaliumbromatlösung ist festzuhalten.
- 8.8. Die Lösung wird auf Zimmertemperatur abgekühlt, 2 g Kaliumjodid (4.5) zugegeben und durchgemischt.
- 8.9. Das gebildete Jod wird mit 0,1 N Natriumthiosulfatlösung (4.11) titriert. Zum Abschluß der Titration werden einige Tropfen Stärkelösung (4.12) als Indikator zugesetzt. Die verbrauchte Menge Natriumthiosulfat (b) ist festzuhalten.
- 9. BERECHNUNG
Der Gehalt an Zinkphenolsulfonat der Probe oder des Rückstands (6) wird in Massenprozent (% m/m) mittels folgender Formel berechnet:
hierbei ist
a | = | Gesamtverbrauch in ml an 0,1 N Kaliumbromatlösung (8.7), |
b | = | Verbrauch an 0,1 N Natriumthiosulfatlösung für die Rücktitration in ml (8.9), |
m | = | Einwaage der Probe (des Rückstands) in g (8.1), |
V1 | = | Volumen der nach 8.2 erhaltenen Lösung in ml, |
V2 | = | Volumen des für die Analyse verwendeten gelösten Abdampfrückstands (8.4) in ml. |
Bemerkung
Bei Aerosolen muß das Meßergebnis in % (m/m) des Rückstands (6) auf das ursprüngliche Erzeugnis umgerechnet werden.
- 10. WIEDERHOLBARKEIT (1)
Bei einem Gehalt von etwa 5% Zinkphenolsulfonat darf der Unterschied zwischen den Ergebnissen von 2 Parallelbestimmungen an der gleichen Probe nicht mehr als 0,5% relativ betragen.
- 11. INTERPRETATION DER MESSERGEBNISSE
Nach der Richtlinie für kosmetische Mittel dürfen Gesichtswässer und Deodorantien höchstens 6% (m/m) Zinkphenolsulfonat enthalten. Aufgrund dieser Vorschrift muß neben dem Gehalt an Phenolsulfonsäure auch der Gehalt an Zink bestimmt werden. Multipliziert man den berechneten (9) Gehalt an Zinkphenolsulfonat mit dem Faktor 0,1588, dann wird der Zinkgehalt in % (m/m) erhalten, der aufgrund des gemessenen Gehalts an Phenolsulfonsäure mindestens in dem Erzeugnis enthalten sein muß. Der tatsächliche, gravimetrisch bestimmte Zinkgehalt – siehe die entsprechende Vorschrift kann jedoch höher sein, da zur Herstellung kosmetischer Mittel auch Zinkchlorid und/oder Zinksulfat verwendet werden darf.
_______________
(1) Siehe Norm ISO/DIS 5725.
Zuletzt aktualisiert am
09.05.2017
Gesetzesnummer
10010899
Dokumentnummer
NOR12138651
alte Dokumentnummer
N8199547958J
Zusatzdokumente: image001, image002, image003
Lizenziert vom RIS (ris.bka.gv.at - CC BY 4.0 DEED)