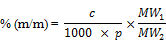Anlage 35
NACHWEIS UND BESTIMMUNG VON HEXAMIDEN, DIBROMHEXAMIDIN, DIBROMPROPAMIDIN UND CHLORHEXIDIN
- 1. Zweck und Anwendungsbereich
Diese Methode beschreibt ein Verfahren zum Nachweis und zur Bestimmung von
- Hexamidin und dessen Salzen einschließlich Isethionat und p-Hydroxybenzoat,
- Dibromhexamidin und dessen Salzen einschließlich Isethionat,
- Dibrompropamidin und dessen Salzen einschließlich Isethionat,
- Chlorhexidindiacetat, -digluconat und -dihydrochlorid
in kosmetischen Erzeugnissen.
- 2. Definition
Der nach diesem Verfahren ermittelte Gehalt an Hexamidin, Dibromhexamidin, Dibrompropamidin und Chlorhexidin wird in Massenprozent (% m/m) des Erzeugnisses angegeben.
- 3. Kurzbeschreibung
Die qualitative und quantitative Bestimmung erfolgt mit Hilfe der Ionenpaar-HPLC mit reverser Phase und nachfolgender UV-Spektrophotometrie. Hexamidin, Dibromhexamidin, Dibrompropamidin und Chlorhexidin werden über ihre Retentionszeit nachgewiesen.
- 4. Reagenzien
Alle Reagenzien müssen analysenrein und, wo erforderlich, für die HPLC geeignet sein.
- 4.1. Methanol.
- 4.2. Natriumsalz der 1-Heptansulfonsäure, Monohydrat.
- 4.3. Essigsäure (Eisessig, d20 = 1,05 g/ml).
- 4.4. Natriumchlorid.
- 4.5. Fließmittel (Mobile Phase).
- 4.5.1. Eluent I: 0,005 M Lösung des Natriumsalzes der 1-Heptansulfonsäure (4.2) in Methanol (4.1), mit Essigsäure (4.3) auf einen scheinbaren pH-Wert von 3,5 eingestellt.
- 4.5.2. Eluent II: 0,005 M wäßrige Lösung des Natriumsalzes der 1-Heptansulfonsäure (4.2), mit Essigsäure (4.3) auf einen pH-Wert von 3,5 eingestellt.
Bemerkung: | Die Eluenten I und II können erforderlichenfalls zur Verbesserung der Peakform modifiziert und wie folgt hergestellt werden: |
- Eluent I: 5,84 g Natriumchlorid (4.4) und 1,1013 g des Natriumsalzes der 1Heptansulfonsäure (4.2) werden in 100 ml Wasser gelöst. Nach Zusatz von 900 ml Methanol (4.1) wird die Mischung mit Essigsäure (4.3) auf einen scheinbaren pH-Wert von 3,5 eingestellt.
- Eluent II: 5,84 g Natriumchlorid (4.4) und 1,1013 g des Natriumsalzes der 1Heptansulfonsäure (4.2) werden in 1 Liter Wasser gelöst und mit Essigsäure (4.3) auf einen pH-Wert von 3,5 eingestellt.
- 4.6. Hexamidindiisethionat [C20H26N4O2
2C2H6O4S].
- 4.7. Dibromhexamidindiisethionat [C20H24Br2N4O2
2C2H6O4S].
- 4.8. Dibrompropamidindiisethionat [C17H18Br2N4O2
2C2H6O4S].
- 4.9. Chlorhexidindiacetat [C22H30Cl2N10
2C2H4O2].
- 4.10. Referenzlösungen: 0,05%ige (m/v) Lösungen von jedem der vier Konservierungsmittel (4.6 bis 4.9) in Eluent I (4.5.1).
- 4.11. 3,4,4'-Trichlor-carbanilid (Triclocarban).
- 4.12. 4,4'-Dichlor-3-trifluormethyl-carbanilid (Halocarban).
- 5. Geräte
- 5.1. Normale Laborausstattung.
- 5.2. Hochleistungsflüssigkeitschromatograph mit UV-Detektor mit variabler Wellenlänge.
- 5.3. Analytische Trennsäule.
Material: Edelstahl,
Länge: 30 cm,
Innendurchmesser: 4 mm,
Aktiver Festkörper:
-Bondapak C18, 10
m, oder gleichwertiges Erzeugnis.
- 5.4. Ultraschallbad.
- 6. Nachweis
- 6.1. Vorbereitung der Probe
Ungefähr 0,5 g Probe werden in einen 10-ml-Meßkolben eingewogen und mit Eluent I (4.5.1) zur Marke aufgefüllt. Der Meßkolben wird 10 Minuten lang in ein Ultraschallbad (5.4) gestellt. Die Mischung wird anschließend zentrifugiert oder durch ein Faltenfilter filtriert. Die überstehende Flüssigkeit bzw. das Filtrat wird für den Nachweis verwendet.
- 6.2. Chromatographie
- 6.2.1. Gradientenprogramm:
Zeit | Eluent I | Eluent II |
(Minuten) | (4.5.1) (% v/v) | (4.5.2) (% v/v) |
0 | 50 | 50 |
15 | 65 | 35 |
30 | 65 | 35 |
45 | 50 | 50 |
- 6.2.2. Volumenstrom der mobilen Phase (6.2.1): 1,5 ml/min, Säulentemperatur: 35 °C.
- 6.2.3. Detektionswellenlänge: 264 nm.
- 6.2.4. 10
l jeder Referenzlösung (4.10) werden injiziert und die Chromatogramme aufgezeichnet.
- 6.2.5. 10
l der Probelösung (6.1) werden injiziert und das Chromatogramm aufgezeichnet.
- 6.3. Durch Vergleich der Retentionszeiten der nach 6.2.5 aufgezeichneten Peaks mit den nach 6.2.4 ermittelten Retentionszeiten wird das Vorhandensein von Hexamidin, Dibromhexamidin, Dibrompropamidin bzw. Chlorhexidin nachgewiesen.
- 7. Bestimmung
- 7.1. Herstellung der Standardlösungen
Als innerer Standard wird eines der Konservierungsmittel (4.6 bis 4.9), das in der Probe nicht vorhanden ist, verwendet. Ist dies nicht möglich, kann Triclocarban (4.11) oder Halocarban (4.12) verwendet werden.
- 7.1.1. 0,05%ige (m/v) Stammlösung des nach 6.3 identifizierten Konservierungsmittels in Eluent I (4.5.1).
- 7.1.2. 0,05%ige (m/v) Stammlösung des als inneren Standard gewählten Konservierungsmittels in Eluent I (4.5.1).
- 7.1.3. Gemäß nachstehender Tabelle werden für jedes identifizierte Konservierungsmittel vier Standardlösungen hergestellt, indem die entsprechenden Volumina der Stammlösung des identifizierten Konservierungsmittels (7.1.1) und der Stammlösung des inneren Standards (7.1.2) in eine Serie von 10-ml-Meßkolben pipettiert und mit Eluent I (4.5.1) bis zur Marke aufgefüllt und gemischt werden.
- 7.2. Vorbereitung der Probe
- 7.2.1. Ungefähr 0,5 g der Probe (p Gramm) werden in einen 10-ml-Meßkolben genau eingewogen, mit 1,0 ml der Lösung des inneren Standards (7.1.2) und 6 ml Eluent I (4.5.1) versetzt und gemischt.
- 7.2.2. Die Mischung wird 10 Minuten in ein Ultraschallbad (5.4) gestellt und nach dem Abkühlen mit dem Eluenten I (4.5.1) zur Marke aufgefüllt und gemischt. Die Mischung wird anschließend zentrifugiert oder durch ein Faltenfilter filtriert. Die überstehende Flüssigkeit bzw. das Filtrat wird chromatographiert.
- 7.3. Chromatographie
- 7.3.1. Der Gradient und der Volumenstrom der mobilen Phase, die Säulentemperatur und die Detektionswellenlänge werden entsprechend den Bedingungen für den Nachweis (6.2.1 bis 6.2.3) eingestellt.
- 7.3.2. 10
l der Probelösung (7.2.2) werden chromatographiert, die Peakflächen gemessen und das Verhältnis zwischen der Peakfläche des zu bestimmenden Konservierungsmittels und der Peakfläche des inneren Standards ermittelt. Die Wiederholbarkeit des Meßsignals wird durch wiederholtes Chromatographieren überprüft.
- 7.4. Eichung
- 7.4.1. 10
l jeder der vier Standardlösungen (7.1.3) werden chromatographiert und die Peakflächen gemessen.
- 7.4.2. Für jede Standardlösung (7.1.3) wird das Verhältnis zwischen der Peakfläche des Hexamidins, des Dibromhexamidins, des Dibrompropamidins bzw. des Chlorhexidins und der Peakfläche des inneren Standards ermittelt.
Es wird eine Eichkurve gezeichnet, indem die Peakflächenverhältnisse als Ordinate und die entsprechenden Konzentrationen des zu bestimmenden Konservierungsmittels in der Standardlösung in Mikrogramm je Milliliter als Abszisse aufgetragen werden.
- 7.4.3. Aus der Eichkurve (7.4.2) wird die Konzentration des zu bestimmenden Konservierungsmittels abgelesen, die dem nach 7.3.2 ermittelten Peakflächenverhältnis entspricht.
- 8. Berechnung
Der Gehalt an Hexamidin, Dibromhexamidin, Dibrompropamidin oder Chlorhexidin in Massenprozent (% m/m) der Probe wird nach folgender Formel berechnet:
c | = | aus der Eichkurve abgelesene Konzentration des zu bestimmenden Konservierungsmittels der Probelösung in Mikrogramm je Milliliter, |
p | = | Einwaage der untersuchten Probe in Gramm (7.2.1), |
MW1 | = | Molmasse der basischen Form des zu bestimmenden Konservierungsmittels, |
MW2 | = | Molmasse des entsprechenden Salzes (siehe Abschnitt 10). |
- 9. Wiederholbarkeit (1)
Bei einem Gehalt an Hexamidin, Dibromhexamidin, Dibrompropamidin oder Chlorhexidin von 0,1% (m/m) dürfen die Ergebnisse zweier an derselben Probe parallel durchgeführter Bestimmungen um nicht mehr als 0,005% (m/m) voneinander abweichen.
- 10. Molmassen
Hexamidin | C20H26N4O2 | 354,45 |
Hexamidindiisethionat | 606,72 | |
Hexamidin-bis (p-hydroxybenzoat) | 630,71 | |
Dibromhexamidin | C20H24Br2N4O2 | 512,24 |
Dibromhexamidindiisethionat | 764,51 | |
Dibrompropamidin | C17H18Br2N4O2 | 470,18 |
Dibrompropamidindiisethionat | 722,43 | |
Chlorhexidin | C22H30Cl2N10 | 505,45 |
Chlorhexidindiacetat | 625,56 | |
Chlorhexidindigluconat | 897,76 | |
Chlorhexidindihydrochlorid | 578,37 | |
__________
(1) ISO 5725.
Zuletzt aktualisiert am
09.05.2017
Gesetzesnummer
10010899
Dokumentnummer
NOR12138679
alte Dokumentnummer
N8199547986J
Zusatzdokumente: image001, image002, image003, image004, image005, image006
Lizenziert vom RIS (ris.bka.gv.at - CC BY 4.0 DEED)