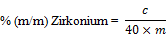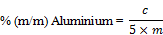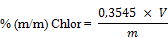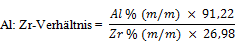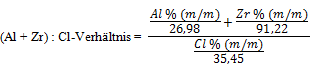Anlage 34
NACHWEIS VON ZIRKONIUM UND BESTIMMUNG VON ZIRKONIUM, ALUMINIUM UND CHLOR IN NICHTAEROSOLFÖRMIGEN ANTITRANSPIRANTIEN
Die Methode umfaßt fünf Schritte:
- A. Nachweis von Zirkonium,
- B. Bestimmung von Zirkonium,
- C. Bestimmung von Aluminium,
- D. Bestimmung von Chlor,
- E. Berechnung des Verhältnisses von Aluminiumatomen zu Zirkoniumatomen sowie von Aluminium- und Zirkoniumatomen zu Chloratomen.
A. Nachweis von Zirkonium
- 1. Zweck und Anwendungsbereich
Diese Methode eignet sich zum Nachweis von Zirkonium in nichtaerosolförmigen Antitranspirantien. Es werden keine Methoden beschrieben, die für den Nachweis des Aluminium-Zirkonium-Chlorid-Hydroxid-Komplexes (AlxZR(OH)yClz
nH2O) geeignet sind.
- 2. Kurzbeschreibung
Zirkonium wird durch den charakteristischen rot-violetten Niederschlag nachgewiesen, der mit Alizarinrot S unter stark sauren Bedingungen entsteht.
- 3. Reagenzien
Alle Reagenzien müssen analysenrein sein.
- 3.1. Salzsäure, konzentriert (d20 = 1,18 g/ml).
- 3.2. Alizarinrot-S-Lösung (Cl. 58005): 2%iges (m/v) wäßriges Natrium-Alizarinsulphonat.
- 4. Geräte
- 4.1. Normale Laborausstattung.
- 5. Arbeitsvorschrift
- 5.1. In einem Reagenzglas werden zu ca. 1 g Probe 2 ml Wasser gegeben. Das Reagenzglas wird verschlossen und geschüttelt.
- 5.2. Es werden 3 Tropfen Alizarinrot-S-Lösung (3.2) und dann 2 ml konzentrierte Salzsäure (3.1) zugegeben. Das Reagenzglas wird verschlossen und geschüttelt.
- 5.3. Das Reagenzglas wird etwa 2 Minuten stehengelassen.
- 5.4. Eine Lösung und ein Niederschlag von rotvioletter Farbe zeigen das Vorhandensein von Zirkonium.
B. Bestimmung von Zirkonium
- 1. Zweck und Anwendungsbereich
Diese Methode eignet sich zur Bestimmung von Zirkonium in Aluminium-Zirkonium-Chlorid-Hydroxid-Komplexen bis zu einer Höchstkonzentration von 7,5 % (m/m) Zirkonium in nichtaerosolförmigen Antitranspirantien.
- 2. Kurzbeschreibung
Zirkonium wird unter sauren Bedingungen aus dem Produkt extrahiert und durch Atomabsorptionsspektroskopie bestimmt.
- 3. Reagenzien
Alle Reagenzien müssen analysenrein sein.
- 3.1. Salzsäure, konzentriert (d20 = 1,18 g/ml).
- 3.2. Salzsäurelösung, 10 % (v/v): zu 500 ml Wasser werden in einem Becherglas unter ständigem Rühren 100 ml konzentrierte Salzsäure (3.1) gegeben. Diese Lösung wird in einen 1-l-Meßkolben geschüttet und bis zur Marke mit Wasser aufgefüllt.
- 3.3. Zirkonium-Maßlösung, 1 000
g/ml in 0,5 M Salzsäurelösung („SpektrosoL“ oder gleichwertiges).
- 3.4. Aluminiumchlorid-Reagenz (hydriert) [AlCl3
6H2O] : 22,6 g Aluminiumchloridhexahydrat werden in 250 ml 10%iger (v/v) Salzsäurelösung (3.2) gelöst.
- 3.5. Ammoniumchloridreagenz: 5,0 g Ammoniumchlorid werden in 250 ml 10%iger (v/v) Salzsäurelösung (3.2) gelöst.
- 4. Geräte
- 4.1. Normale Laborausstattung.
- 4.2. Heizplatte mit Magnetrührer.
- 4.3. Filterpapier (Whatman Nr. 41 oder gleichwertiges).
- 4.4. Atomabsorptionsspektrometer mit Zirkonium-Hohlkathodenlampe.
- 5. Arbeitsvorschrift
- 5.1. Vorbereitung der Probe
- 5.1.1. Ungefähr 1,0 g (m Gramm) einer homogenen Probe des Produkts werden in ein 150-ml-Becherglas sorgfältig eingewogen. Man fügt 40 ml Wasser und 10 ml konzentrierte Salzsäure (3.1) hinzu.
- 5.1.2. Das Becherglas wird auf eine Heizplatte mit Magnetrührer (4.2) gestellt. Der Inhalt wird unter Rühren zum Kochen gebracht. Um rasches Verdunsten zu verhindern, wird das Becherglas mit einem Uhrglas abgedeckt. Nach 5minütigem Kochen wird das Becherglas von der Heizplatte genommen und auf Raumtemperatur abgekühlt.
- 5.1.3. Mit Hilfe des Filterpapiers (4.3) wird der Inhalt des Becherglases in einen 100-ml-Meßkolben filtriert. Das Becherglas wird zweimal mit je 10 ml Wasser gespült, und das Spülwasser wird nach Filtration in den Meßkolben gegeben. Der Meßkolben wird bis zur Marke mit Wasser aufgefüllt und der Inhalt vermischt. Diese Lösung wird auch für die Aluminiumbestimmung verwendet (Teil C).
- 5.1.4. In einen 50-ml-Meßkolben werden 20,00 ml der Probenlösung (5.1.3), 5,00 ml Aluminiumchloridreagenz (3.4) und 5,00 ml Ammoniumchloridreagenz (3.5) pipettiert. Die Lösung wird mit 10%iger (v/v) Salzsäurelösung (3.2) bis zur Marke aufgefüllt und vermischt.
- 5.2. Bedingungen für die Atomabsorptionsspektroskopie
Flamme: Distickstoffoxid/Acetylen,
Wellenlänge: 360,1 nm,
Untergrundkorrektur: nein,
Brennstoff: reich; für maximale Absorption müssen Brennerhöhe und Brennstoff optimiert werden.
- 5.3. Eichung
- 5.3.1. Von der Zirkonium-Maßlösung (3.3) werden 5,00, 10,00, 15,00, 20,00 und 25,00 ml in eine Reihe von 50-ml-Meßkolben pipettiert. In jeden Meßkolben werden 5,00 ml Aluminiumchloridreagenz (3.4) und 5,00 ml Ammoniumchloridreagenz (3.5) pipettiert. Die Lösungen werden mit 10%iger (v/v) Salzsäurelösung (3.2) zur Marke aufgefüllt und vermischt. Sie enthalten 100, 200, 300, 400 bzw. 500
g Zirkonium je Milliliter.
Auf die gleiche Weise wird eine Blindlösung ohne Zirkonium-Maßlösung zubereitet.
- 5.3.2. Die Absorption der Blindlösung (5.3.1) wird gemessen und der erhaltene Wert als Nullpunkt der Zirkoniumkonzentration für die Eichkurve gesetzt. Die Absorption jeder Zirkonium-Eichlösung (5.3.1) wird gemessen. Man zeichnet eine Eichkurve, die den Zusammenhang zwischen Absorptionswerten und Zirkoniumkonzentration aufzeigt.
- 5.4. Bestimmung
Die Absorption der Probenlösung (5.1.4) wird gemessen. Aus der Eichkurve liest man die zugehörige Zirkoniumkonzentration ab.
Berechnung
Der Zirkoniumgehalt der Probe in Massenprozent wird nach folgender Formel berechnet:
Dabei ist:
m = | Masse der zu analysierenden Probe (5.1.1) in Gramm; und |
c = | die aus der Eichkurve abgelesene Zirkoniumkonzentration in der Probenlösung (5.1.4) in Mikrogramm je Milliliter. |
- 7. Wiederholbarkeit (1)
Bei einem Zirkoniumgehalt von 3,00 % (m/m) dürfen die Ergebnisse zweier parallel laufender Bestimmungen an derselben Probe nicht mehr als 0,10 % (m/m) voneinander abweichen.
- 8. Anmerkungen
Statt der Atomabsorptionsspektroskopie kann auch eine ICP-Emissionsspektroskopie durchgeführt werden.
C. Bestimmung von Aluminium
- 1. Zweck und Anwendungsbereich
Diese Methode eignet sich zur Bestimmung von Aluminium in Aluminium-Zirkonium-Chlorid-Hydroxid-Komplexen bis zu einer Höchstkonzentration von 12 % (m/m) Aluminium in nichtaerosolförmigen Antitranspirantien.
- 2. Kurzbeschreibung
Aluminium wird unter sauren Bedingungen aus dem Produkt extrahiert und mit Hilfe der Atomabsorptionsspektroskopie bestimmt.
- 3. Reagenzien
Alle Reagenzien müssen analysenrein sein.
- 3.1. Salzsäure, konzentriert (d20 = 1,18 g/ml).
- 3.2. Salzsäurelösung 1 % (v/v): zu 500 ml Wasser werden in einem Becherglas unter ständigem Rühren 10 ml konzentrierte Salzsäure (3.1) gegeben. Die Lösung wird in einen 1-l-Meßkolben geschüttet und bis zur Marke mit Wasser aufgefüllt.
- 3.3. Aluminium-Maßlösung, 1 000
g/ml in 0,5 M Salpetersäurelösung („SpektrosoL“ oder gleichwertiges).
- 3.4. Kaliumchloridreagenz: 10,0 g Kaliumchlorid werden in 250 ml 1%iger (v/v) Salzsäurelösung (3.2) gelöst.
- 4. Geräte
- 4.1. Normale Laborausstattung.
- 4.2. Atomabsorptionsspektrometer mit Aluminium-Hohlkathodenlampe.
- 5. Arbeitsvorschrift
- 5.1. Vorbereitung der Probe
Zur Bestimmung des Aluminiumgehalts wird die gemäß B 5.1.3 zubereitete Lösung verwendet.
- 5.1.1. In einen 100-ml-Meßkolben werden 5,00 ml der Probenlösung (B 5.1.3) und 10,00 ml Kaliumchloridreagenz (3.4) pipettiert. Die Lösung wird mit 1%iger (v/v) Salzsäurelösung (3.2) bis zur Marke aufgefüllt und vermischt.
- 5.2. Bedingungen für die Atomabsorptionsspektroskopie
Flamme: Distickstoffoxid/Acetylen,
Wellenlänge: 309,3 nm
Untergundkorrektur: nein,
Brennstoff: reich; für maximale Absorption müssen Brennerhöhe und Brennstoff optimiert werden.
- 5.3. Eichung
- 5.3.1. Von der Aluminium-Maßlösung (3.3) werden 1,00, 2,00, 3,00, 4,00 und 5,00 ml in eine Reihe von 100-ml-Meßkolben pipettiert. In jeden Meßkolben werden 10,00 ml Kaliumchloridreagenz (3.4) pipettiert. Die Lösungen werden mit 1%iger (v/v) Salzsäurelösung (3.2) zur Marke aufgefüllt und vermischt. Sie enthalten 10, 20, 30, 40 und 50
g Aluminium je Milliliter.
Auf die gleiche Weise wird eine Blindlösung ohne Aluminium-Maßlösung zubereitet.
- 5.3.2. Die Absorption der Blindlösung (5.3.1) wird gemessen und der erhaltene Wert als Nullpunkt der Aluminiumkonzentration für die Eichkurve gesetzt. Die Absorption jeder Aluminiumeichlösung wird gemessen. Man zeichnet eine Eichkurve, die den Zusammenhang zwischen Absorptionswerten und Aluminiumkonzentration aufzeigt.
- 5.4. Bestimmung
Die Absorption der Probenlösung (5.1.1) wird gemessen. Aus der Eichkurve liest man die zugehörige Aluminiumkonzentration ab.
- 6. Berechnung
Der Aluminiumgehalt der Probe in Massenprozent wird nach folgender Formel berechnet:
Dabei ist:
m = | Masse der zu analysierenden Probe (B. 5.1.1) in Gramm; und |
c = | die aus der Eichkurve abgeleseneAluminiumkonzentration in der Probenlösung (5.1.1) in Mikrogramm je Milliliter. |
- 7. Wiederholbarkeit (1)
Bei einem Aluminiumgehalt von 3,5 % (m/m) dürfen die Ergebnisse zweier parellel laufender Bestimmungen an derselben Probe nicht mehr als 0,10 % (m/m) voneinander abweichen.
- 8. Anmerkungen
Statt der Atomabsorptionsspektroskopie kann auch eine ICP-Emissionsspektroskopie durchgeführt werden.
D. Bestimmung von Chlor
- 1. Zweck und Anwendungsbereich
Diese Methode eignet sich zur Bestimmung von Chlor, das als Chlorid-Ion in Aluminium-Zirkonium-Chlorid-Hydroxid-Komplexen in nichtaerosolförmigen Antitranspirantien vorliegt.
- 2. Kurzbeschreibung
Der Chloridgehalt im Produkt wird durch potentiometrische Titration mit Hilfe von Silbernitrat-Maßlösung bestimmt.
- 3. Reagenzien
Alle Reagenzien müssen analysenrein sein.
- 3.1. Salpetersäure, konzentriert (d20 = 1,42 g/ml).
- 3.2. Salpetersäurelösung, 5 % (v/v): zu 250 ml Wasser werden in einem Becherglas unter ständigem Rühren 25 ml konzentrierte Salpetersäure (3.1) gegeben. Die Lösung wird in einen 500-ml-Meßkolben geschüttet und bis zur Marke mit Wasser aufgefüllt.
- 3.3. Aceton.
- 3.4. Silbernitrat, 0,1 M Maßlösung („AnalaR“ oder gleichwertiges).
- 4. Geräte
- 4.1. Normale Laborausstattung.
- 4.2. Heizplatte mit Magnetrührer.
- 4.3. Silberelektrode.
- 4.4. Calomel-Bezugselektrode.
- 4.5. pH/Millivoltmeter, das für potentiometrische Titration geeignet ist.
- 5. Arbeitsvorschrift
- 5.1. Vorbereitung der Probe
- 5.1.1. Ungefähr 1,0 g (m Gramm) einer homogenen Probe des Produkts werden in ein 250-ml-Becherglas sorgfältig eingewogen. Man fügt 80 ml Wasser und 20 ml 5%ige (v/v) Salpetersäurelösung (3.2) hinzu.
- 5.1.2. Das Becherglas wird auf eine Heizplatte mit Magnetführer (4.2) gestellt. Der Inhalt wird unter Rühren zum Kochen gebracht. Um schnelles Austrocknen zu verhindern, wird das Becherglas mit einem Uhrglas abgedeckt. Nach 5minütigem Kochen wird das Becherglas von der Heizplattegenommen und auf Raumtemperatur abgekühlt.
- 5.1.3. Man fügt 10 ml Aceton (3.3) hinzu, taucht die Elektroden (4.3 und 4.4) in die Lösung und beginnt zu rühren. Man titriert potentiometrisch mit 0,1 M Silbernitratlösung (3.4) und zeichnet eine Differentialkurve zur Bestimmung des Endpunkts (V ml).
- 6. Berechnung
Der Chlorgehalt der Probe in Massenprozent wird nach folgender Formel berechnet:
Dabei ist:
m = | Masse der zu analysierenden Probe (5.1.1) in Gramm; und |
V = | Volumen des bis zum Endpunkt der Titration (5.1.3) verbrauchten 0,1 M Silbernitrats in Milliliter. |
Wiederholbarkeit (1)
Bei einem Chlorgehalt von 4 % (m/m) dürfen die Ergebnisse zweier parallel laufender Bestimmungen an derselben Probe nicht mehr als 0,10 % (m/m) voneinander abweichen.
E. Berechnung des Verhältnisses von Aluminiumatomen zu Zirkoniumatomen sowie von Aluminium- und Zirkoniumatomen zu Chloratomen
- 1. Berechnung des Verhältnisses von Aluminiumatomen zu Zirkoniumatomen
Das Al: Zr-Verhältnis wird nach folgender Formel berechnet:
- 2. Berechnung des Verhältnisses von Aluminium- und Zirkoniumatomen zu Chloratomen
Das (Al + Zr): Cl-Verhältnis wird nach folgender Formel berechnet:
___________
(1) ISO 5725.
Zuletzt aktualisiert am
09.05.2017
Gesetzesnummer
10010899
Dokumentnummer
NOR12138678
alte Dokumentnummer
N8199547985J
Zusatzdokumente: image001, image002, image003, image004, image005, image006, image007, image008
Lizenziert vom RIS (ris.bka.gv.at - CC BY 4.0 DEED)