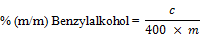Anlage 33
NACHWEIS UND BESTIMMUNG VON BENZYLALKOHOL IN KOSMETISCHEN MITTELN
A. Nachweis
- 1. Zweck und Anwendungsbereich
Diese Methode beschreibt ein Verfahren zum Nachweis von Benzylalkohol in kosmetischen Mitteln.
- 2. Kurzbeschreibung
Die Identifizierung erfolgt durch Dünnschichtchromatographie auf Kieselgelplatten.
- 3. Reagenzien
Alle Reagenzen (Anm.: richtig: Reagenzien) müssen analysenrein sein.
- 3.1. Benzylalkohol.
- 3.2. Chloroform.
- 3.3. Absolutes Ethanol.
- 3.4. n-Pentan.
- 3.5. Fließmittel: Diethylether.
- 3.6. Benzylalkohol-Standardlösung: 0,1 g Benzylalkohol (3.1) wird in einen 100-ml-Meßkolben eingewogen, mit Ethanol (3.3) bis zur Marke aufgefüllt und gemischt.
- 3.7. DC-Fertigplatten (Glas, 200 mm x 200 mm oder 100 mm x 200 mm).
Adsorbensschicht: Kieselgel 60 F254.
Schichtdicke: 0,25 mm.
- 3.8. Sprühreagenz: 12-Molybdatophosphorsäure, 10% (m/v) in Ethanol (3.3).
- 4. Geräte:
- 4.1. Übliche Ausrüstung zur Dünnschichtchromatographie.
- 4.2. Doppeltrogkammer, Gesamtmaße ungefähr 80 x 230 x 240 mm.
- 4.3. Chromatographiepapier: Whatman oder gleichwertiges.
- 4.4. UV-Lampe, Wellenlänge 254 nm.
- 5. Durchführung
- 5.1. Vorbereitung der Probe
1,0 g der zu untersuchenden Probe wird in einen 10-ml-Meßkolben eingewogen. Nach Zusatz von 3 ml Chloroform (3.2) wird bis zur gleichmäßigen Verteilung der Probe geschüttelt. Die Mischung wird mit Ethanol (3.3) bis zur Marke aufgefüllt und kräftig geschüttelt, bis sich eine klare oder nahezu klare Lösung ergibt.
- 5.2. Dünnschichtchromatographie
- 5.2.1. Die Doppeltrogkammer (4.2) wird mit n-Pentan (3.4) wie folgt gesättigt: Die Kammerwand des hinteren Troges wird mit Chromatographiepapier (4.3) ausgelegt, wobei der untere Rand des Papiers in den Trog hineinreicht. 25 ml n-Pentan (3.4) werden durch Gießen über die sichtbare Oberfläche des Chromatographiepapiers in den hinteren Trog eingefüllt. Anschließend wird die Kammer sofort mit dem Deckel verschlossen und 15 Minuten stehengelassen.
- 5.2.2. 10
l der Probelösung (5.1) und 10
l Benzylalkohol-Standardlösung (3.6) werden auf die Dünnschichtplatte an geeigneten Punkten entlang der Startlinie aufgetragen.
- 5.2.3. In den vorderen Trog der Kammer werden 10 ml Fließmittel (3.5) pipettiert und anschließend sofort die Dünnschichtplatte (5.2.2) in denselben Trog hineingestellt. Der Kammerdeckel wird sofort wieder aufgesetzt und die Dünnschichtplatte bis zu einer Höhe von 150 mm entwickelt. Die Dünnschichtplatte wird der Kammer entnommen und bei Raumtemperatur aufbewahrt, bis das Fließmittel verdunstet ist.
- 5.2.4. Die Dünnschichtplatte (5.2.3) wird im ultravioletten Licht der Wellenlänge 254 nm betrachtet; die violetten Flecke werden markiert. Anschließend wird die Dünnschichtplatte mit dem Sprühreagenz (3.8) besprüht und danach ungefähr 15 Minunten (Anm.: richtig: Minuten) lang bei 120 °C erhitzt. Benzylalkohol erscheint als dunkelblauer Fleck.
- 5.2.5. Der Rf-Wert des Benzylalkohol-Standards wird berechnet. Das Chromatogramm zeigt bei Vorhandensein von Benzylalkohol in der Probelösung einen dunkelblauen Fleck mit dem RfWert und der Farbe des Fleckes der Benzylalkohol-Standardlösung.
B. Bestimmung
- 1. Zweck und Anwendungsbereich
Diese Methode beschreibt ein Verfahren zur Bestimmung von Benzylalkohol in kosmetischen Mitteln.
- 2. Definition
Der nach diesem Verfahren bestimmte Gehalt an Benzylalkohol wird in Massenprozent (% m/m) ausgedrückt.
- 3. Kurzbeschreibung
Die Probe wird mit Methanol extrahiert und der Gehalt an Benzylalkohol im Extrakt durch Hochleistungsflüssigkeitschromatographie (HPLC) bestimmt.
- 4. Reagenzien
Alle Reagenzien müssen analysenrein und, wo erforderlich, für die HPLC geeignet sein.
- 4.1. Methanol.
- 4.2. 4-Ethoxyphenol.
- 4.3. Benzylalkohol.
- 4.4. Fließmittel (Mobile Phase): Methanol (4.1)/Wasser (45 : 55; v/v).
- 4.5. Benzylalkohol-Stammlösung: Ungefähr 0,1 g Benzylalkohol (4.3) wird genau in einen 100-ml-Meßkolben eingewogen, mit Methanol (4.1) gelöst, zur Marke aufgefüllt und gemischt.
- 4.6. Stammlösung des inneren Standards: Ungefähr 0,1 g 4-Ethoxyphenol (4.2) wird genau in einen 100-ml-Meßkolben eingewogen, mit Methanol (4.1) gelöst, bis zur Marke aufgefüllt und gemischt.
- 4.7. Standardlösungen: Gemäß nachstehender Tabelle werden die entsprechenden Volumina der Benzylalkohol-Stammlösung (4.5) und der Stammlösung des inneren Standards (4.6) in eine Serie von 25-ml-Meßkolben einpipettiert und mit Methanol (4.1) bis zur Marke aufgefüllt und gemischt.
Standard- | Benzylalkohol | 4-Ethoxyphenol | ||
(4.5) | (4.6) | |||
I | 0,5 | 20 | 2,0 | 80 |
II | 1,0 | 40 | 2,0 | 80 |
III | 2,0 | 80 | 2,0 | 80 |
IV | 3,0 | 120 | 2,0 | 80 |
V | 5,0 | 200 | 2,0 | 80 |
(*) Diese Werte sind richtungsweisend und entsprechen den Konzentrationen in den bereiteten Standardlösungen, wenn Lösungen von Benzylalkohol (4.5) und 4-Ethoxyphenol (4.6) verwendet werden, die genau 0,1% (m/v) Benzylalkohol bzw. genau 0,1% (m/v) 4‑Ethoxyphenol enthalten. | ||||
- 5. Geräte
- 5.1. Normale Laborausstattung.
- 5.2. Hochleistungsflüssigkeitschromatograph (HPLC) mit Ultra-violett-Detektor mit variabler Wellenlänge und mit 10
l Probenschleife.
- 5.3. Analytische Trennsäule:
Material: Edelstahl,
Länge: 25 cm,
Innendurchmesser: 4,6 mm,
Aktiver Festkörper: 5
m Spherisorb ODS oder gleichwertiges Erzeugnis.
- 5.4. Wasserbad.
- 5.5 Ultraschallbad.
- 5.6. Zentrifuge.
- 5.7. Zentrifugengläser mit 15 ml Fassungsvermögen.
- 6. Durchführung
- 6.1. Vorbereitung der Probe
- 6.1.1. Ungefähr 0,1 g (m Gramm) der Probe wird genau in ein Zentrifugenglas (5.7) eingewogen und mit 5 ml Methanol (4.1) versetzt.
- 6.1.2. Die Mischung wird 10 Minuten im 50 °C warmen Wasserbad (5.4) erwärmt und anschließend in ein Ultraschallbad (5.5) bis zur homogenen Verteilung gestellt.
- 6.1.3. Nach dem Abkühlen wird die Mischung 5 Minuten bei 3 500 U/min zentrifugiert.
- 6.1.4. Die überstehende Flüssigkeit wird in einen 25-ml-Meßkolben übergeführt.
- 6.1.5. Der Rückstand wird mit weiteren 5 ml Methanol (4.1) extrahiert. Die Extrakte werden im 25-ml-Meßkolben vereinigt.
- 6.1.6. Nach Zusatz von 2,0 ml Stammlösung des inneren Standards (4.6) mittels Pipette wird mit Methanol (4.1) zur Marke aufgefüllt und gemischt. Diese Lösung wird, wie im Abschnitt 6.4 beschrieben, chromatographiert.
- 6.2. Bedingungen für die Chromatographie
- 6.2.1. Volumenstrom der mobilen Phase: 2 ml/min.
- 6.2.2. Detektionswellenlänge: 210 nm.
- 6.3. Eichung
- 6.3.1. 10
l jeder der fünf Benzylalkohol-Standardlösungen (4.7) werden chromatographiert und die Peakflächen des Benzylalkohols und des 4-Ethoxyphenols gemessen.
- 6.3.2. Für jede Konzentration der Benzylalkohol-Standardlösungen (4.7) wird das Verhältnis zwischen der Peakfläche des Benzylalkohols und der Peakfläche des 4-Ethoxyphenols ermittelt. Es wird eine Eichkurve gezeichnet, indem die Peakflächenverhältnisse als Ordinate und die entsprechenden Konzentrationen des Benzylalkohols in Mikrogramm je Milliliter als Abszisse aufgetragen werden.
- 6.4. Bestimmung
- 6.4.1. 10
l der Probelösung (6.1.6) werden chromatographiert, die Peakflächen des Benzylalkohols und des 4-Ethoxyphenols gemessen und das Peakflächenverhältnis von Benzylalkohol zu 4Ethoxyphenol ermittelt. Die Wiederholbarkeit des Meßsignals wird durch wiederholtes Chromatographieren überprüft.
- 6.4.2. Aus der Eichkurve (6.3.2) wird die Konzentration des Benzylalkohols abgelesen, die dem Peakflächenverhältnis von Benzylalkohol zu 4-Ethoxyphenol entspricht.
- 7. Berechnung
Der Benzylalkoholgehalt in Massenprozent (m/m) der Probe wird nach folgender Formel berechnet:
m = | Einwaage der untersuchten Probe im Gramm (6.1.1), |
c = | aus der Eichkurve abgelesene Konzentration an Benzylalkohol der Probelösung (6.1.6) in Mikrogramm je Milliliter. |
- 8. Wiederholbarkeit (1)
Bei einem Benzylalkoholgehalt von 1 % (m/m) dürfen die Ergebnisse zweier an derselben Probe parallel durchgeführter Bestimmungen um nicht mehr als 0,10 % (m/m) voneinander abweichen.
__________
(1) ISO 5725.
Zuletzt aktualisiert am
09.05.2017
Gesetzesnummer
10010899
Dokumentnummer
NOR12138677
alte Dokumentnummer
N8199547984J
Zusatzdokumente: image001, image002, image003, image004
Lizenziert vom RIS (ris.bka.gv.at - CC BY 4.0 DEED)