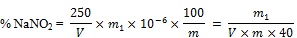Anlage 10
III. NACHWEIS UND QUANTITATIVE BESTIMMUNG VON NITRIT
A. NACHWEIS
- 1. ANWENDUNGSBEREICH
Die Methode kann zum Nachweis von Nitrit in kosmetischen Erzeugnissen verwendet werden, insbesondere in Cremes, Salben und Zahnpasten.
- 2. PRINZIP DER METHODE
Nitrit wird durch die Bildung von gefärbten Reaktionsprodukten von 2-Aminobenzaldehyd-phenylhydrazon (Nitrin) nachgewiesen.
- 3. REAGENZIEN
Es sind analysenreine Reagenzien zu verwenden.
- 3.1. Verdünnte Schwefelsäure: Verdünne 2 ml konzentrierte Schwefelsäure
(d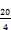
- 3.2. Verdünnte Salzsäure: Verdünne 1 ml konzentrierte Salzsäure
(d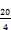
- 3.3. Methanol
- 3.4. Lösung von 2-Aminobenzaldehyd phenylhydrazon (Nitrin) in Methanol.
Wiege 2 g Nitrin in einen 100-ml-Meßkolben. Füge tropfenweise 4 ml verdünnte Salzsäure (3.2) hinzu und schüttle. Fülle bis zur Marke mit Methanol auf und mische bis die Lösung völlig klar ist. Die Lösung wird in einer braunen Glasflasche aufbewahrt (4.3).
- 4. GERÄTE
- 4.1. Becherglas 50 ml
- 4.2. 100-ml-Meßkolben
- 4.3. 125 ml braune Glasflasche
- 4.4. Glasplatte, 10 x 10 cm
- 4.5. Kunststoffspatel
- 4.6. Filtrierpapier, 10 x 10 cm
- 5. DURCHFÜHRUNG
- 5.1. Verstreiche einen Teil der zu untersuchenden Probe gleichmäßig auf der Glasplatte, bis zu einer Dicke von nicht mehr als 1 cm.
- 5.2. Tränke ein Blatt Filterpapier (4.6) in destilliertem Wasser, lege dieses auf die Probe und drücke das Filterpapier mit einem Plastikspatel an (4.5).
- 5.3. Warte einige Minuten und benetze die Mitte des Filterpapiers:
erst mit 2 Tropfen verdünnter Schwefelsäure (3.1),
dann mit 2 Tropfen von der Nitrinlösung (3.4).
- 5.4. Nach 5 bis 10 Sekunden entferne das Filtrierpapier und betrachte es gegen Tageslicht. Die Anwesenheit von Nitrit wird durch eine purpurrote Färbung angezeigt.
Bei niedrigen Nitritkonzentrationen verändert sich die purpurrote Farbe nach 5 bis 15 Sekunden in gelb. Wenn hohe Nitritkonzentrationen vorhanden sind, tritt die Farbveränderung erst nach 1 bis 2 Minuten ein.
- 6. BEMERKUNG
Die Intensität der purpurroten Farbe und die Zeit bis zur Farbveränderung gibt einen Hinweis auf den Nitritgehalt der Probe.
B. BESTIMMUNG
- 1. ANWENDUNGSBEREICH
Die Methode beschreibt die Bestimmung von Nitrit in kosmetischen Erzeugnissen.
- 2. BEGRIFFSBESTIMMUNG
Der Nitritgehalt der Probe, bestimmt nach dieser Methode, wird in % (m/m) Natriumnitrit angegeben.
- 3. PRINZIP DER METHODE
Die Probe wird mit Wasser verdünnt und geklärt. Das Nitrit wird mit Sulfanilamid und N-1-Naphthyläthylen-Diamin in Reaktion gebracht und die entstehende Färbung bei 538 nm gemessen.
- 4. REAGENZIEN
Es sind analysenreine Reagenzien zu verwenden.
- 4.1. Klärlösungen: Diese Lösungen sind wöchentlich frisch herzustellen.
- 4.1.1. Carrez-I-Reagenz:
106 g Kaliumzyanoferrat (II), K4Fe(CN)6
3H2O in destilliertem Wasser auflösen und auf 1 000 ml verdünnen.
- 4.1.2. Carrez-II-Reagenz:
219,5 g Zinkazetat, Zn (CH3COO)2
2H2O und 30 ml Eisessig in destilliertem Wasser auflösen und auf 1 000 ml verdünnen.
- 4.2. Natriumnitritlösung:
0,500 g Natriumnitrit in destilliertem Wasser auflösen und auf 1 000 ml verdünnen. Danach 10 ml dieser Stammlösung auf 500 ml verdünnen. 1 ml Lösung = 10 Mikrogramm NaNO2.
- 4.3. 1 N Natriumhydroxidlösung:
4,0 g NaOH in destilliertem Wasser auflösen und auf 100 ml verdünnen.
- 4.4. 0,2%-Sulfanilamid-Hydrochloridlösung:
2,0 g Sulfanilamid in 800 ml Wasser durch Erwärmen auflösen. Abkühlen, 100 ml konzentrierte Salzsäure unter Rühren hinzufügen und auf 1 000 ml verdünnen.
- 4.5. 5-n-Salzsäure:
445 ml konzentrierte Salzsäure
(d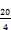
- 4.6. N-1-Naphthyläthylendiamin-Dihydrochloridreagenz
(Naphthylreagenz):
Die Lösung ist täglich frisch herzustellen.
0,1 g N-1-Naphthyläthylendiamin-Dihydrochlorid in Wasser auflösen und auf 100 ml verdünnen.
- 5. GERÄTE UND HILFSMITTEL
- 5.1. Analytische Waage
- 5.2. 100-, 250-, 500- und 1 000-ml-Meßkolben
- 5.3. Vollpipetten oder Meßpipetten
- 5.4. 100-ml-Meßzylinder
- 5.5. Faltenfilter, nitritfrei, Durchmesser 15 cm
- 5.6. Wasserbad
- 5.7. Spektrophotometer mit 1-cm-Küvetten
- 5.8. pH-Meßgerät
- 5.9. 10-ml-Mikrobürette
- 5.10. 250-ml-Becherglas
- 6. DURCHFÜHRUNG
- 6.1. Wiege ungefähr 5 g der homogenisierten Probe auf 0,1 mg genau ein. Überführe sie mit heißem destilliertem Wasser quantitativ in einen 250-ml-Kolben und bringe das Volumen auf ungefähr 150 ml mit heißem destilliertem Wasser. Erwärme den Kolben 1/2 Stunde lang in einem Wasserbad von 80 °C. Während dieser Zeit ist gelegentlich umzuschütteln.
- 6.2. Kühle auf Raumtemperatur ab und füge nacheinander unter Umrühren 2 ml Carrez I (4.1.1) und 2 ml Carrez II (4.1.2) zu.
- 6.3. Bringe mit 1-N-Natronlauge (4.3) auf pH 8,3 (pH-Meßgerät benutzen). Überführe den Inhalt quantitativ in einen 250-ml-Meßkolben und fülle zur Marke mit destilliertem Wasser auf.
- 6.4. Vermische den Inhalt und filtriere durch ein Faltenfilter (5.5).
- 6.5. Pipettiere einen angemessenen aliquoten Teil (V ml) des klaren Filtrats, aber nicht mehr als 25 ml, in einen 100-ml-Meßkolben und fülle destilliertes Wasser bis zu einem Volumen von 60 ml hinzu.
- 6.6. Nach dem Durchmischen füge 10 ml Sulfanilamid-Hydrochloridlösung (4.4) und dann 6 ml der 5-n-Salzsäure (4.5) zu. Mische und lasse 5 Minuten stehen. Füge 2 ml des N-1-Naphthyläthylendiaminreagenz (4.6) hinzu, mische und lasse 3 Minuten stehen. Fülle bis zur Marke mit Wasser auf und schüttele durch.
- 6.7. Zur Herstellung einer Blindprobe wiederhole die Operationen nach 6.5 und 6.6 ohne Hinzufügung des N-1-Naphthylreagenz (4.6).
- 6.8. Bestimme (5.7) die Extinktion bei 538 nm, dabei ist der Blindwert nach 6.7 als Vergleich zu verwenden.
- 6.9. Entnehme aus der Eichkurve (6.10) den Natriumnitritgehalt in Mikrogramm pro 100 ml der Lösung (m1 Mikrogramm), die der nach 6.8 gemessenen Extinktion entspricht.
- 6.10. Unter Verwendung der 10
g/ml Natriumnitritlösung (4.2) wird eine Eichkurve für die Konzentrationen 0, 20, 40, 60, 80, 100
g Natriumnitrit pro 100 ml hergestellt.
- 7. BERECHNUNG
Berechne den Gehalt an Natriumnitrit in % (m/m) nach folgender Formel:
Dabei bedeuten
m | = | Masse der für die Untersuchung eingesetzten Probemenge in g (6.1), |
m1 | = | Natriumnitritgehalt in Mikrogramm, ermittelt nach 6.9, |
V | = | ml-Filtrat verwendet für die Messung (6.5). |
- 8. WIEDERHOLBARKEIT (1)
Für einen Gehalt von ungefähr 0,2 % m/m Natriumnitrit darf die Differenz zwischen zwei Parallelbestimmungen den absoluten Wert von 0,005 % nicht überschreiten.
____________
(1) Siehe Norm ISO 5725.
Zuletzt aktualisiert am
09.05.2017
Gesetzesnummer
10010899
Dokumentnummer
NOR12138654
alte Dokumentnummer
N8199547961J
Zusatzdokumente: image001, image002, image003, image004
Lizenziert vom RIS (ris.bka.gv.at - CC BY 4.0 DEED)